人乳腺癌细胞MCF7保留了分化乳腺上皮的许多特性。包括:能通过胞质雌激素受体加工雌二醇并能形成圆形复合物(domes)。该细胞含有WNT7B癌基因。肿瘤坏死因子α(TNF alpha)可以压制MCF-7细胞生长。细胞经抗雌激素处理后能调节胰岛素样生长因子结合蛋白IGFBPS分泌。
中乔新舟培养体系
MEM(含NEAA)(中乔新舟 货号:ZQ-300)+10%胎牛血清(中乔新舟 货号:AU0600)+1%双抗(中乔新舟 货号:CSP006)+1%L-alanyl-L-glutamine(中乔新舟 货号:CSP004)+1%SP(中乔新舟 货号:CSP003)+0.01%human recombinant insulin(中乔新舟 货号:CSP001-10)
1. 胰岛素是由胰岛β细胞分泌的一种多肽激素。胰岛素是无血清哺乳动物细胞培养基中的普遍添加物质;
2. 在许多细胞活动中发挥重要作用:如促进糖和氨基酸转运,提高合成代谢降低分解代谢,刺激细胞生长等等。重组人胰岛素为重组技术生产的由51个氨基酸残基组成的多肽;
3. 培养时,人胰岛素可以代替牛胰岛素;
4. 中乔新舟的胰岛素为白色或类白色结晶性粉末,在水、乙醇和乙醚中几乎不溶,在稀盐酸和稀氢氧化钠溶液中易溶。本产品用10mM盐酸溶液溶解制成10mg/ml的浓缩液,经0.22μm过滤除菌,可作为哺乳动物贴壁细胞或悬浮细胞培养添加剂,使用时请根据细胞培养要求添加。
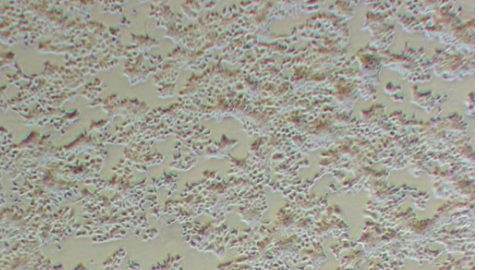
MCF-7特点
倍增时间:1.8天(PubMed=9671407);80小时(PubMed=25984343);31.2小时(PubMed=22628656);25.3小时(PubMed=24389870);25.4小时(NCI-DTP)~50小时,范围为30-72小时(DSMZ)~38小时(PBCF);
成团簇的形式生长:
由于mcf-7细胞是三维团簇的方式生长,复苏和传代后会重新附着为三维岛(会有一些不会重新附着的簇)。生长最终会从岛屿状慢慢扩散开来,随着时间的推移,细胞会缓慢变成单层,这个时候细胞基本处于对数生长期。
生长缓慢:
倍增时间:1.8天(PubMed=9671407);80小时(PubMed=25984343);31.2小时(PubMed=22628656);25.3小时(PubMed=24389870);25.4小时(NCI-DTP)~50小时,范围为30-72小时(DSMZ)~38小时(PBCF)。
传代比例:
MCF-7是一种本身生长缓慢的细胞,当细胞培养至细胞 70-80% 的汇合度,即可进行分瓶处理,一般T25培养瓶建议1:2传代,每周可传代一次,如果细胞生长速度比正常的时候更慢,可以适当提高血清到20%有利于促进生长。
贴壁率低:
该细胞在复苏、传代后,细胞会有一些漂浮状态,这些漂浮细胞是正常现象,可以视为混合的贴壁和悬浮细胞系。一般复苏、传代培养3天后漂浮细胞会再继续粘附贴壁。直到生长从岛屿扩散开来并且在培养瓶内伸展开,通常在进行换液的时候我们会补加培养基,如果一定要全换液,可以通过离心收集悬浮细胞以1000转5min,并将悬浮细胞接种到新培养瓶。
密度依耐性:
Mcf-7细胞密度低时,生长缓慢,接种密度建议启动接种密度:8.0 x 10 4至 1.5 x 10 5活细胞/cm 2为宜;继代培养的接种密度:4.0 x 10 4 至 1.0 x 10 5 活细胞/cm 2。
收货后处理技巧
冻存管MCF-7:
收到货后确保泡沫箱是否有干冰,若无干冰及时拍照并反馈中乔新舟销售或技术;
如果细胞不急用可放入-80冰箱一周,长期保持请放入液氮哦;
复苏建议离心去除冻存液,快速加入提前准加入培养液的复苏瓶;
显微镜下观察细胞亮度及密度,必要时可进行取样了解存活率;
放入培养箱后2-3天再次观察,如果漂浮细胞属于正常情况,请耐性等待。
复苏瓶MCF-7:
收到货后喷放入培养箱静止2-4小时;
显微镜下观察细胞状态并进行拍照;
细胞几乎都贴壁的情况下进行传代处理;
消化过程中加入胰酶手掌心拍打瓶尾部,细胞成片脱落后,可稍微延长30s-60s,至细胞呈现单个细胞即可终止。
实验高分文章
1.MCF-7 cells(货号:ZQ0071,影响因子:14.919)。
Bacteria eat nanoprobes for aggregation-enhanced imaging and killing diverse microorganisms原文链接:
https://www.nature.com/articles/s41467-022-28920-6
2.MCF-7 cells(货号:ZQ0071,影响因子:11.78)。
A metabolic acidity-activatable calcium phosphate probe with fluorescence signal amplification capabilities for non-invasive imaging of tumor malignancy原文链接:
https://www.sciencedirect.com/science/article/pii/S2095927321006952
 上海中乔新舟生物科技有限公司
上海中乔新舟生物科技有限公司